Le Rêve Ultime en Cristallisation : Contrôler la Pureté, la Taille et la Forme de Cristaux !
Publié par German Montes Hernandez, le 3 mai 2026 320
La capacité à contrôler la pureté, la taille et la forme de cristaux constitue l'un des défis majeurs de la cristallisation, dont l'un des principaux objectifs est de produire des phases spécifiques de haute pureté selon les besoins. Les processus de bio-minéralisation en sont d'excellents exemples car les organismes sont capables de sélectionner des polymorphesa spécifiques avec une précision parfaite.
a un cristal qui peut prendre plusieurs formes et capable de se transformer physico-chimiquement en modifiant son apparence
Dans les processus de nucléation et de croissance des cristaux, le polymorphisme est un phénomène très courant dans les milieux naturels mais aussi dans les processus de production industrielle. Ce phénomène peut également avoir un impact significatif sur les procédés de fabrication et les produits (par exemple, les médicaments). En laboratoire ou dans l'industrie, différents polymorphes peuvent être générés en utilisant des conditions opératoires spécifiques, en recourant à divers solvants, en fonction de la présence ou de l'absence d'impuretés, en appliquant différentes conditions hydrodynamiques des fluides, par une étape de vieillissement hydro-thermique (température de maturation) ou simplement avec le temps (temps de maturation). C’est pour cela que la capacité à contrôler la phase polymorphe souhaitée est l'un des défis ultimes de la cristallisation, dont l'objectif principal est de produire des phases spécifiques de haute pureté avec une taille et forme selon les besoins d’usage. Les meilleurs exemples de contrôle des polymorphes proviennent du domaine de la bio-minéralisation, où les organismes peuvent sélectionner des polymorphes spécifiques avec une fidélité parfaite.
En ce qui concerne les carbonates de calcium (CaCO3), trois polymorphes existent : la calcite (cristaux en forme de rhomboèdres, scalénoèdres et parfois prismatiques), l’aragonite (cristaux prismatiques allongées, prismes hexagonaux et souvent aussi des masses fibreuses) et la vatérite (agrégats en forme sphérulites souvent en forme de « fleurs » constitués de nanocristaux en aiguilles). La synthèse de ces trois polymorphes est parfaitement contrôlées par les organismes vivants tel que les coquilles marines mais leur synthèse et contrôle en laboratoire sous conditions de chimie douce sans aide des organismes vivants (conditions abiotiques) restaient jusqu’à présent encore un défi. En effet, 20 ans de recherche depuis mon arrivée à Grenoble ont été nécessaire pour arriver à maitriser la pureté, la forme et la taille de carbonates de calcium sous conditions abiotiques en m’inspirant des connaissances actuelles en bio-minéralisation. Dans ce contexte, j’ai porté plusieurs études, publiées depuis 20071. Mais c’est grâce à un dispositif expérimental de suivi en temps réel par spectroscopie Raman et à l’imagerie électronique à haute résolution que j’ai développé à ISTerre2 (publié en 2016) qu’actuellement, il est possible de synthétiser des nanoparticules de calcite, de vaterite agrégées en forme de chou-fleur3 et des microparticules d’aragonite en forme de fibres ou de grains de riz (Figure 1 ci-dessous).

Figure 1. Synthèse abiotique des polymorphes de carbonates de calcium par chimie douce à pression-température ambiante et sans aide des organismes vivants et/ou sans additifs organiques (voir sources 2-4).
Dans la littérature scientifique, l'aragonite et la vatérite ont été moins étudiés que la calcite. Cette dernière étant le carbonate de calcium le plus stable dans des conditions normales de pression et de température3. Dans le contexte de la biominéralisation, le polymorphe de l'aragonite se forme parfaitement dans plusieurs coquillages et coraux ; cependant, son mécanisme de formation reste encore mal compris et a fait l'objet de débats. Sa formation dans des conditions abiotiques en laboratoire a généralement été contrôlée par la température (60-90 °C) et par la présence de Mg et/ou de molécules organiques. Cependant, la nucléation et/ou la synthèse de l'aragonite à température ambiante (T < 30 °C) dans des conditions abiotiques restait un défi majeur, maintenant résolu à ISTerre en combinant simplement la chimie du Ca et Mg en milieu aqueux (voir Figure 2 ci-dessous).

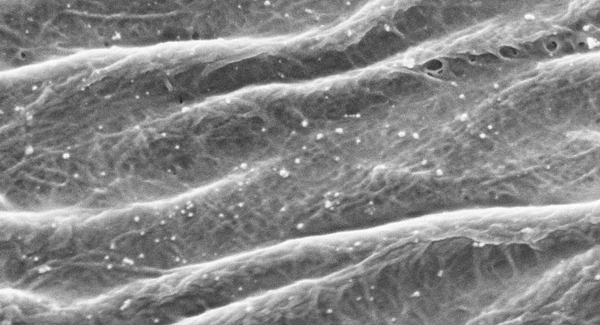
Figure 2. Synthèse d'aragonite en forme de grains de riz (image microscopie électronique, FESEM) par la transformation de monohydrocalcite en milieu aqueux à la température de la pièce (environ 25°C) et pression atmosphérique (article scientifique en révision).
Ces études ont ainsi permis de trouver des pistes concises sur la formation de la dolomite4, un minéral énigmatique pour les géologues et chimistes « expérimentateurs » (voir aussi la source 4).
En effet, la surveillance en temps réel à l'aide d'outils analytiques diversifiés comme la diffusion des rayons X (SAXS/WAXS), la spectroscopie d'absorption des rayons X (EXAFS/XANES), la microscopie à force atomique et microscopie électronique (AFM et TEM), ou encore la spectroscopie Raman sans oublier la simulation numérique avancée ont considérablement contribué à l'état actuel des connaissances sur les processus de nucléation de cristaux au cours des dernières décennies. De nos jours, on admet de plus en plus la formation de phases amorphes et/ou cristallines transitoires aux premiers stades du processus de cristallisation d'un cristal ou d'un minéral métastable ou stable. Ce chemin de cristallisation est conforme à la règle d’Ostwald, mais les phases transitoires (germes ou clusters, matière colloïdale, gels, phases amorphes et cristallines) ne sont pas nécessairement des polymorphes. En effet, elles peuvent présenter des compositions chimiques et des tailles de particules différentes.
En résumé, les mesures en temps réel pour sonder la naissance des phases cristallines permettent de mieux comprendre et ainsi être capable de contrôler la pureté, la taille et la forme de cristaux.
Sources :
(1) G. Montes-Hernandez, F. Renard, N. Geffroy, L. Charlet, J. Pironon, Calcite precipitation from CO2-H2O-Ca(OH)2 slurry under high pressure of CO2. Journal of Crystal Growth 308 (2007) 228-236.
Calcite precipitation from CO2–H2O–Ca(OH)2 slurry under high pressure of CO2 - ScienceDirect
(2) G. Montes-Hernandez, F. Renard. Time-resolved in situ Raman spectroscopy of the nucleation and growth of siderite, magnesite and calcite and their precursors. Crystal Growth & Design 16 (2016) 7218-7230.
(3) Carlos Pimentel, German Montes-Hernandez, Pablo Almarza-Cifuentes, Matthias Kellermeier, Alexander E.S. Van Driessche. From Waste to Value : Conversion of Calcium Sulfate to Vaterite via Carbon Capture and Storage. Advanced Functional Materials, 2026 ; 0:e19977
(4) G. Montes-Hernandez, F. Renard, A.L. Auzende, N. Findling. Amorphous calcium-magnesium carbonate (ACMC) accelerates dolomitization at room temperature under abiotic conditions. Crystal Growth & Design 20 (2020) 1434-1441.