Les nanotechnologies appliquées au traitement du cancer
Publié par Sandy Aupetit, le 21 avril 2016 17k
Première cause de décès prématuré avant 65 ans, le cancer est une maladie redoutée. En 2015, près de 385 000 nouveaux cas ont été déclarés. D'après les statistiques, un homme sur deux et une femme sur trois se verra diagnostiquer un cancer au cours de sa vie.
Mais finalement, c'est quoi un cancer ?
Pour le savoir, il va falloir nous intéresser à la biologie cellulaire, et comprendre tout d'abord comment notre corps fonctionne en temps normal. Il faut savoir que le corps contient des centaines de milliards de cellules, qui forment les tissus et les organes. La plupart de ces cellules ont une durée de vie limitée : quelques jours pour les cellules de la paroi des intestins à quelques mois pour les globules rouges du sang. Tous les jours, des cellules se divisent donc pour remplacer les cellules mortes. Ce processus est étroitement contrôlé. Une cellule ne commence à se diviser que si elle en reçoit l’ordre, via des signaux chimiques appelés « facteurs de croissance ». De plus, chaque cellule possède une sorte de programme interne d’autodestruction. Il se déclenche en cas d’anomalie de la cellule et provoque sa destruction en quelques heures. Finalement, ce sont tous ces processus qui permettent à notre organisme de conserver son équilibre.
Quand le système dérape...
Seulement, il arrive parfois que certaines cellules perdent leur capacité de croissance contrôlée. Elles n’attendent plus les signaux externes leur indiquant de croitre ou se diviser, leur programme d’autodestruction s’est enrayé, et rien ne va plus. Résultat, elles se divisent trop rapidement et croissent de façon désordonnée, formant une grosseur appelée tumeur.
Pour autant, si la prolifération s’arrête, ce n’est pas un cancer mais un phénomène bénin, toutes les tumeurs ne sont pas cancéreuses. Mais dans un certain nombre de cas, la tumeur peut évoluer vers un carcinome, c’est- à-dire un cancer localisé. Quand les cellules continuent à se diviser de façon anarchique, la tumeur locale grossit au détriment des tissus et des organes sains avoisinants.
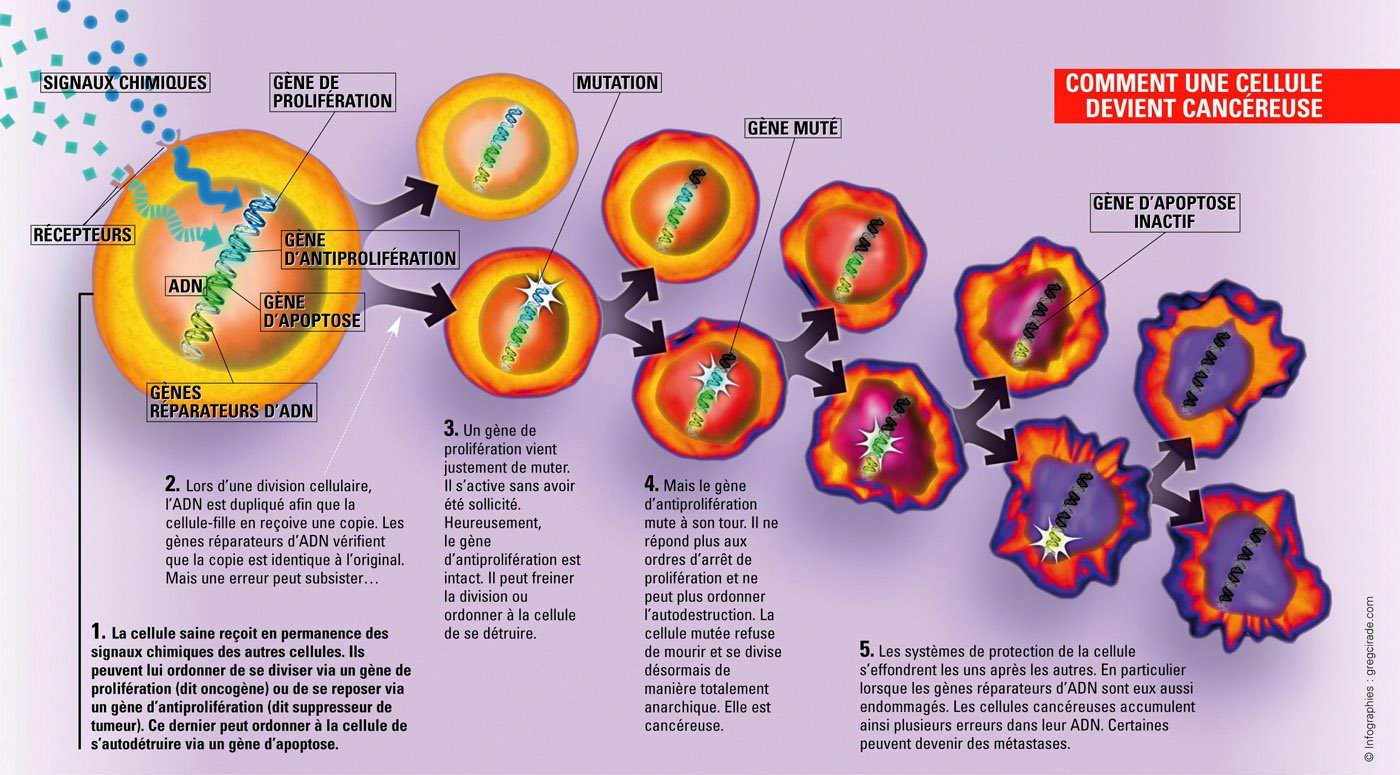
Schéma représentant les différentes étapes menant à l'apparition de cellules cancéreuses.
Source : www.gregcirade.com © Greg Cirade
Comment se développe la tumeur ?
Pour pouvoir se développer, la tumeur va provoquer la formation de nouveaux vaisseaux sanguins qui viendront l’irriguer et l’alimenter en oxygène et en nutriments. Ce dernier point est capital car sans irrigation sanguine, la tumeur ne pourrait pas grossir au-delà d’un dixième de millimètre.
Mais ces vaisseaux sanguins vont également poser un autre problème. Les cellules tumorales vont en effet finir par passer dans le système sanguin via ces vaisseaux, et diffuser dans d’autres parties de l’organisme, pour y former de nouvelles tumeurs. C’est ce qu’on appelle les métastases. A ce moment la, le cancer devient invasif.
Ainsi, même si une tumeur cancéreuse initiale est enlevée, la maladie peut récidiver. Cette capacité de diffusion dans l’organisme fait qu’il est essentiel de détecter le plus tôt possible une tumeur et de déterminer si elle est bénigne ou maligne. Dans tous les cas, de nombreux traitements sont possibles dès que le diagnostic est posé, en vue de maîtriser la maladie.
Quels sont les traitements possibles ?
Dans le cadre de cet article nous allons nous intéresser au traitement le plus courant qui est la chimiothérapie. L’idée est d’utiliser des molécules toxiques spécifiquement dirigées contre les cellules de l'organisme qui se multiplient à un rythme très élevé, celles-là mêmes qui sont à l'origine des tumeurs. Ces molécules vont littéralement aller « attaquer » les cellules malades.
Un traitement peu ciblé avec de nombreux effets secondaires
L’inconvénient principal de ce type de traitement vient du fait qu’il n’est pas précisément ciblé. Car les cellules cancéreuses ne sont pas les seules à se développer très rapidement. C'est également le cas des cellules de la moelle osseuse qui fabrique les globules sanguins, des cellules du tube digestif ou des follicules pileux à l'origine des cheveux. La chimiothérapie est donc susceptible de détruire des cellules saines en même temps que les cellules cancéreuses visées, impliquant des effets secondaires comme une fatigue intense, des vomissements ou la chute des cheveux, qui peuvent être particulièrement lourds pour le malade.
Et les nanotechnologies dans tout ça ?
Les nanoparticules peuvent justement aider à mieux cibler le traitement. L’idée est en fait de s’en servir comme véhicules pour transporter les médicaments directement vers les cellules cancéreuses. On veut en quelques sorte construire des livreurs de médicaments ! Ce principe s’appelle la vectorisation.
Plusieurs types de nano-véhicules
On peut lister à ce jour trois principaux types de nano-véhicules :
- Les liposomes : Il faut s’imaginer des ballons de baudruche remplis d’eau, d’une taille d’environ 100nm, c’est-a-dire 70 fois plus petit qu'un globule rouge. Le principe actif du médicament à transporter est dissous soit dans la paroi du ballon, soit dans l’eau.
- Les nanocapsules : Elles sont plus rigides et ressemblent plutôt à des ballons de foot, au cœur duquel le médicament est dissous.
- Les nanosphères : Elles s'apparentent quant à elles à des pelotes de laine. Le médicament est en fait piégé dans un enchevêtrement de chaînes de molécules.
Cibler les cellules cancéreuses
Il faut savoir que l'environnement d'une cellule cancéreuse, ou plus globalement d'une tumeur, est un peu différent de celui des cellules saines.
Par exemple, on a pu remarquer que le pH au niveau d’une tumeur est de l’ordre de 6, tandis que celui des cellules saines est d’environ 7,5. Ces valeurs correspondent typiquement aux pH de l’eau gazeuse et de l’eau plate. Concrètement, cela veut dire qu’au niveau d’une tumeur, le milieu est un peu plus « acide » qu’au niveau des cellules saines. De plus, les cellules cancéreuses possèdent de nombreux marqueurs biologiques spécifiques.
Ce sont toutes ces caractéristiques propres aux cellules malades qui peuvent nous permettre de les repérer et de guider les nanovecteurs.
Le voyage des nano-véhicules dans l'organisme
Alors une fois injectés dans l'organisme, que se passe-t-il pour nos vecteurs ? Prenons l’exemple des liposomes, ces petits ballons de baudruche remplis d’eau décrits tout à l’heure. Lorsqu’ils sont injectés dans la circulation sanguine, notre système immunitaire va réagir à cette intrusion. Ils sont vite reconnus par des protéines nommées opsonines, les gardes du corps de l’organisme, qui vont les étiqueter comme étant inconnus. Ainsi les macrophages situés dans le foie, qui sont quant à eux les éboueurs de l’organisme, sont alertés, et capturent ces éléments. Nos ballons sont alors percés et détruits, libérant le principe actif du médicament.
Ces liposomes dit de "première génération" vont donc principalement être utilisés pour cibler le foie. Pour atteindre d’autres organes, il faudrait qu’ils arrivent à passer incognito pour ne pas se faire détruire au niveau du foie et rester plus longtemps dans la circulation sanguine. Pour cela les scientifiques ont conçu des liposomes de « deuxième génération ». L’idée est de modifier les liposomes classiques en leur greffant des polymères appelés polyéthylène glycol, une sorte de tenue de camouflage qui va leur permettre de ne pas être reconnus par l’organisme. Ils peuvent ainsi passer le barrage des macrophages et atteindre d’autres organes.
Pour aller encore plus loin, il existe également des liposomes de "troisième génération", capables de cibler encore plus efficacement les tumeurs cancéreuses, grâce à des molécules accrochées à leur tenue de camouflage, qui reconnaissent certains marqueurs connus des cellules cancéreuses.
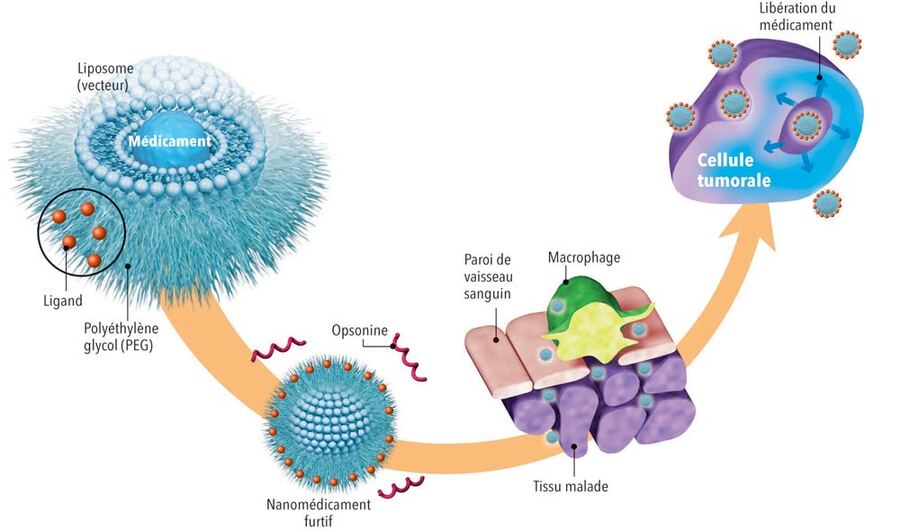
Schéma illustrant le voyage dans l'organisme d'un liposome de troisième génération.
Source : http://www.infographie-illustration.fr/sante/
Publié dans "La Recherche" © Philippe Mouche
Les recherches autour de ces nanovecteurs sont en cours, et les perspectives sont prometteuses, toujours dans l’optique de pouvoir cibler de plus en plus précisément les cellules cancéreuses, et ainsi rendre les traitements moins lourds pour les patients.
Ré-écoutez l'intégralité de l'émission ici :